旅スタディ
- 抗マラリア薬(詳細)
- 抗マラリア薬(簡易)
- 界面化学と洗濯
- 繊維の種類
- 感染性の下痢
- 満月の夜
- 目薬選び
- 旅の予防接種
- 女神の星、金星
- 恒星は、瞬く
- 太陽直径=2分
- 雲は、白い
- 夕陽は、赤い
- 空は、青い
- 真夜中の太陽
©2006-11 Kazuto&Azusa
界面化学と洗濯
旅の間は、いつもいつも手洗濯ばかりです。楽しくないと洗濯は時に苦痛ですから、楽しく洗濯するために、界面化学を分かりやすく把握しておこうと思いました。物理化学の基礎事項だけでまとめていますので、旅人も主婦も、是非ご一読ください♪
■表面張力surface tensionの発生メカニズム
(1)<左図>水中の分子は、あらゆる方向から水分子の引力を受けるので、その力が相殺され、エネルギーをもたない。
(2)<右図>水表面の分子は、左右下に引力を受けるが、上方向の引力を受けない。その力の和は、下方向のエネルギーとなる。
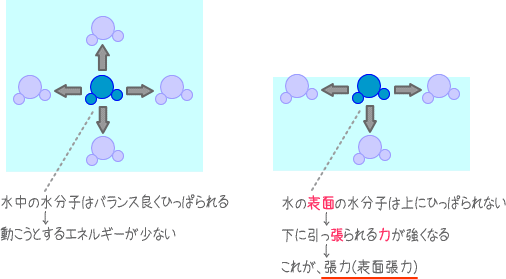
つまり、表面張力は、「空気と反対方向に働く引力」のようなものです。それは「表面・張る・力」の文字通り、「表面を引っ張る力」でもあります。
★ここがとても大事ですよ→「表面を引っ張る力」があれば「表面が延びない」、つまり、「表面積が小さくなる」ことになります。
そう、表面張力は、表面積を小さくする力なのです。日常生活の中では、<左図>雨が粒になり、<右図>コップの表面が盛り上がる、などで観察されますね。

ちなみに水の表面張力は日常の温度では約73dyne/cm・・・数値ではなかなかピンとこないけれど、この数値は、この世の液体の中では水銀に次いで2番目に高いものとなっています(なるほど、水銀は確かに丸まりやすいですね)。
■表面張力と毛細管現象で汗と砂を落とす
洗濯に必要なことは、(1)汗などの塩分を溶かしだすこと、(2)砂などの固形の汚れを除去すること、(3)油(脂)汚れを除去すること、です。
そのためには、まず、衣類の繊維に水を吸い込ませなければなりません。
水は表面張力が大きいので、繊維に吸い上げられて水面が延びると、「表面積を小さくしなければ」という力(表面張力)が働き、その結果水面が上がります。そうしてまた繊維に吸い上げられては水面が上昇し・・・この連続で、水は繊維の隙間をぐんぐんと浸透していくわけです。私たちはこれを毛細管現象として知っています。
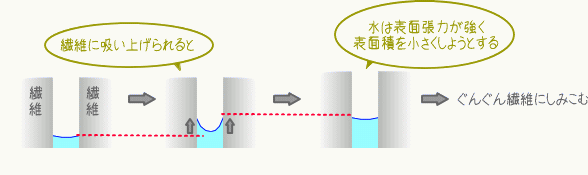
上の説明から「浸透力は、表面張力が大きな液体ほど大きい」ことが理解できます。つまり、「衣類に水分を浸透させるなら真水が良い」「つけおき洗いで、最初に漬ける液体は、真水」ということになります。後述しますが、洗剤の溶液は表面張力が著しく低下しているので、毛細管現象が弱くなるのです。
(物理化学の成書では、毛細管現象で浸透する液面上昇度h=2Scosθ/gρr、つまり表面張力Sに比例するという公式でも説明されています・・・薄い記憶ですが、ワッシュバーン式・・・と言ったような・・・???)
真水が衣類の繊維に浸透したら、(1)の塩分を溶かしだすこともできますし、砂と繊維の間に水が流れ込めば、(2)の繊維にひっかかっている砂を除去することも容易になります。
■表面張力を下げて油(脂)を落とす
先ほど、「つけおき洗いには、真水」と紹介しました。
ところで旅をしていると、皮脂が相当衣類に付着します。もう一つ、移動中バスやトラックに乗っていると排気ガスを浴び、燃料(ガソリンやディーゼル)の微細な油滴が衣類に付着します。洗濯では、脂と油を落とすことが大変に重要です。
水と空気の界面では表面張力が大きすぎるけれど、これが、水と油の界面になると水の表面張力が低下します。分離型ドレッシングで水層と油層の境目がぐにょんぐにょんとしているのは、油に接している水は表面積を小さくする力(表面張力)が弱くなっている証拠そのもの。
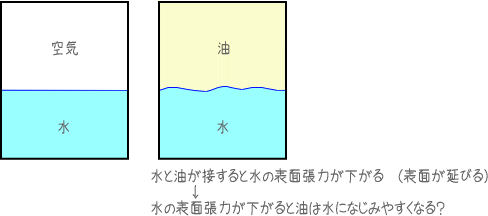
ということは、油を水に溶かしだすには、もっともっともっと表面張力が下がればいい・・・!
洗剤(界面活性剤は)、水の表面張力を激減させる作用があります。界面活性剤は水に溶けない部分を持っており、それゆえ水の“表面に配列”する性質(正吸着)があるので、冒頭で紹介した「空気と反対方向に引っ張られる水分子」を、空気の方向に引っ張ってくれるのです。そうすれば、水は表面を引っ張る力(表面張力)を失います。
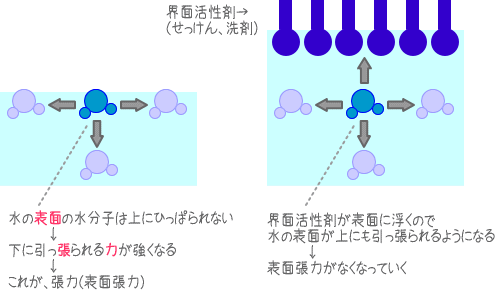
表面張力の低下は、表面積を小さくする力の低下であり、イコール、表面積を大きくする作用と言い換えることができます。水の表面積が大きくなるのだから水はどんどん面積を増し、それが“泡”といった現象で観察されるのです。
水と油の界面も、界面活性剤が入ることによって水の表面積が伸びるようになれば、水はどんどん油と混じり合おうとすることができますよね。
つまり、「つけおき洗いで油汚れを浮かせるには、洗剤の入った水が良い」ということになります。日常生活でも理解できることです。ただしここには注意事項が1つあります。
■表面張力を上げる物質は、大敵
先ほど、「つけおき洗いには、洗剤の入った水」と紹介しました。洗剤(界面活性剤)が表面張力を低下させて油と混じり合う力が生まれるからです。
ここで大敵なのは、「表面張力を上げる物質」です。洗剤と反対の力をもつ物質を混ぜたら、洗剤の効果が相殺されてしまう・・・。そして、その物質とは、ずばり「塩分」なのです。
塩分の代表として、汗や尿の成分である塩化ナトリウム(NaCl)で説明します。塩分は、ご存知の通り水によく溶けます。よく溶けるということは水の内部に存在するので、その引力は表面の水分子を更に内部へ引っ張ってしまうのです。
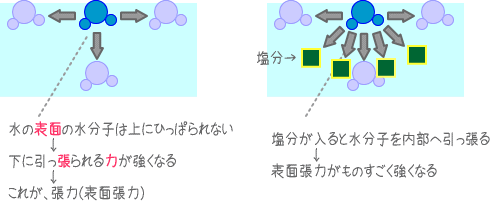
この力は、真水以上に大きな表面張力となり、塩分を含む水は表面が延びなくなってしまいます。つまり「洗剤は、塩分を含む水では効果がでない」ということになります。私たちはこれを、例えば海水浴の後ではシャンプーが泡立たないといった現象で知っています。
★だから、つけおき洗いの原則は、
・まず真水でつけおき→(1)汗などの塩分を溶かしだす、(2)砂などの固形の汚れを除去する
・次に洗剤の入った水→(3)油(脂)汚れを浮かせる
もし洗剤の入った水からつけおきを開始しても、洗剤の作用が汗の塩分で相殺されてしまうので、効果が出なくなってしまうから、この順序はとても大事です。
■油(脂)を落とす、最低必要洗剤量について
さて、なにしろ油は水に溶けないので、これを繊維から引き剥がすのはたーいへん。そのためには、油を洗剤の成分で包み込んでしまいましょう。
先ほど、洗剤の成分は水の表面に配列する(正吸着)を紹介しました。洗剤濃度を高くすればより多くの洗剤分子が水の表面に配列します。そして、その“限界”を超えると・・・洗剤分子は水に溶けない部分を水から背けるようにして水の内部に集まりはじめます。ちょっと難しい言葉で、この“限界”の洗剤量を臨界ミセル濃度と呼んだりもしますが、まあ、難しいですよね。そしてその量を超えて洗剤を溶かすと、洗剤の集合体(会合体)の中には油がはまりやすくなり、油がどんどんと繊維から離れていけるのです。
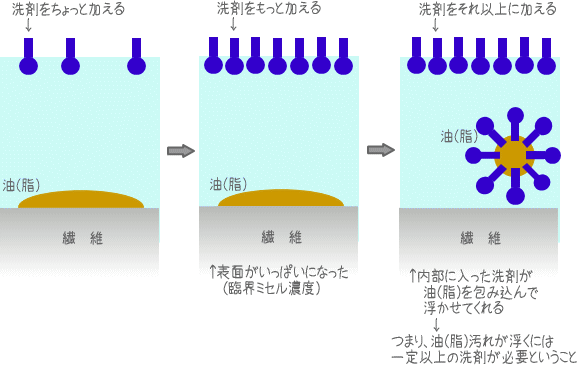
だから、洗濯の原則は、
・油を落とすための必要量があることを知っておく。つまり、洗剤をケチらない。
■まとめ・・・手洗濯のコツ
以上をまとめます。
1)最初は水でつけおき
・衣類に水分を浸透させる
・塩分を溶かしだす
・砂と繊維の絡みを緩める
2)強い力ですすぐ
・砂をここで落としておく
・繊維をこすりあわせるのではない(砂やほこりが繊維に絡まるだけだからNG)
・洗濯機をイメージし、流水で砂を繊維から引き剥がすようする
3)真水ですすぎ、しぼる
・洗剤の大敵である塩分を除去する
・すすぎの後はしっかりしぼる→繊維に水が残ると次の洗剤液が入ってこない
4)次に洗剤を入れてつけおき
・油を浮かせる
・浮いた油を除くため、つけおきの水は捨てる
5)洗濯は、洗剤をケチらない
・一定以上の量の洗剤を使い、油を包み込んで除去する
・“一定量”は洗剤の種類によっても温度によっても違うので、感覚で覚えていくしかない
・もちろん多く入れれば良いというものでもないので注意
毎日手洗濯って、結構面倒に感じることがあるんですよね。でも旅人ならそれは避けられないことだし、どうせ面倒ながらも手洗濯するなら効果的に行いたいものです。何より自分自身が、洗濯を楽しめるようにと、このページをギニアのコナクリで作成しはじめ、ちまちまと、そしてガーナのクマシで完成しました。
19Jan2008